撰稿 / 蔡宜靜 (科學推展中心特約編輯)

圖1. 涂熊林與陳玉如博士研究團隊研發之一站式蛋白體檢驗平台
蛋白質是生物體調控生命網路最重要的系統之一,透過解析細胞層級之表型與訊息路徑的蛋白質表現及修飾之差異性,我們可以探索在不同狀態下細胞的生理變化,從中尋找正常生化反應或異常的調控因子,以應用於疾病檢測或治療。蛋白質體是開發新穎檢測或治療的關鍵,但現今的分析技術除了前置樣品處理繁瑣之外,分析過程也相當複雜,不僅需要數以萬計以上的樣品細胞,從採樣到病理報告出爐更需要長達一週以上的時間。涂熊林博士與陳玉如博士攜手中研院國際研究學程學生宋方寧(Sofani Gebreyesus)、史昂德(Asad Siyal)等團隊成員,利用創新的客製化微流體晶片(iProChip)簡化樣品前處理流程,並結合高靈敏度及可靠的質譜偵測方法,突破現代分析瓶頸,為蛋白質體的研究向前邁出重要的步伐。
蛋白質體—更勝遺傳譯碼,生化反應實際執行者
隨著基因定序研究成果出爐,科學家揭開了基因結構中遺傳密碼的神秘面紗,也確立了基因遺傳密碼組與生命體間至關重要的聯結性。但相較於基因,蛋白質往往是真正參與生化反應及細胞功能的執行者,因此,蛋白質體學:研究生物體內所有蛋白質的學科,變成了生命科學領域最重要的研究課題之一。然而蛋白質體不僅種類、數量龐大,還會經由轉錄及轉譯反應作用,複雜程度遠遠高於基因體。在蛋白質體的研究中,繁瑣的前置處理流程會對分析物造成大量的損耗,因此需要採集大量的細胞樣品,此外,數百萬計且濃度差異極大的胜肽片段對檢測儀器靈敏度也存在嚴格要求,而涂熊林與陳玉如博士帶領研究團隊研發的一站式蛋白質體工作站,成功降低蛋白質體研究對樣品數量的需求,且在具高可靠度條件下,提升檢測靈敏度。
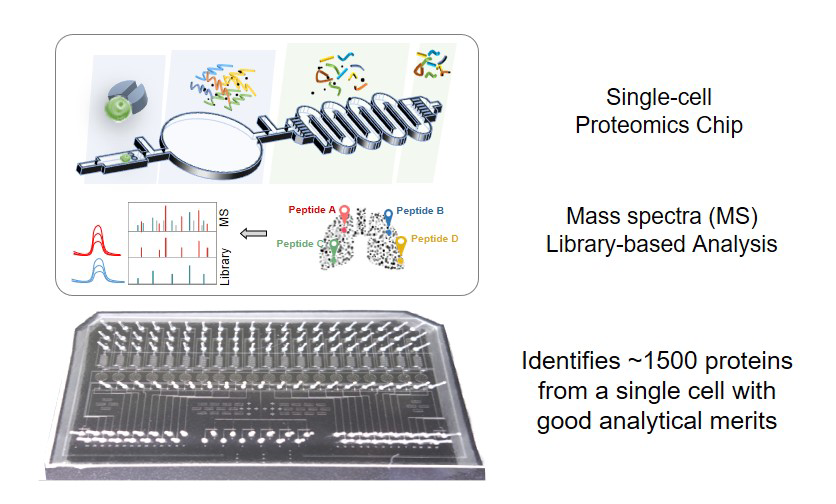
圖2. 涂熊林與陳玉如博士研究團隊,結合客製化微流體晶片與質譜儀分析技術開發精簡且高靈敏的單細胞蛋白質體分析平台。
iProChip—樣品前置處理整合平台
精簡樣品前置處理流程及樣品損耗量,是一站式蛋白質體檢測的關鍵,涂熊林博士研究團隊利用微流體晶片設計,針對不同的分析樣品,建構客製化晶片、通道閥門、晶片材質,在單一晶片上完成樣品細胞捕獲、影像擷取、蛋白質及分析胜肽收集等複雜處理流程,顯著改善單一細胞層級樣品製備效率、減少樣品損耗率,以利後續連接非數據依賴擷取質譜儀進行鑑定與定量。
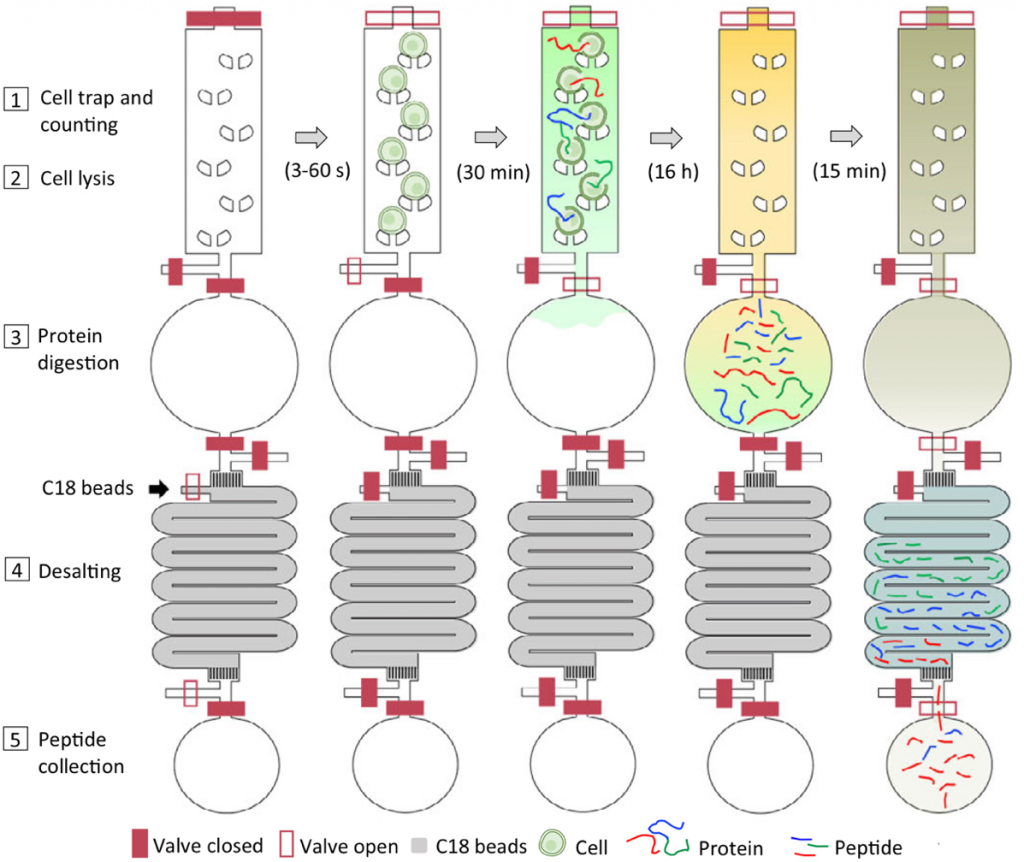
圖3. 微流體新穎晶片iProChip功能設計:1.細胞捕獲,2.細胞裂解,3.蛋白質處理,4.除鹽,5.胜肽蒐集
以肺癌細胞(Non-Small-Cell Lung Cancer, NSCLC) PC-9實驗結果為例,研究團隊設計數量為10、50、100個捕捉槽的iProChip,單一細胞捕獲效率分別100%、92 ± 3%、89 ± 8%,當考慮細胞抓取總量(包含2-3個/捕捉槽)時,其細胞捕獲效率則皆可達100%,展現iProChip晶片充分的細胞層級樣品採集能力。
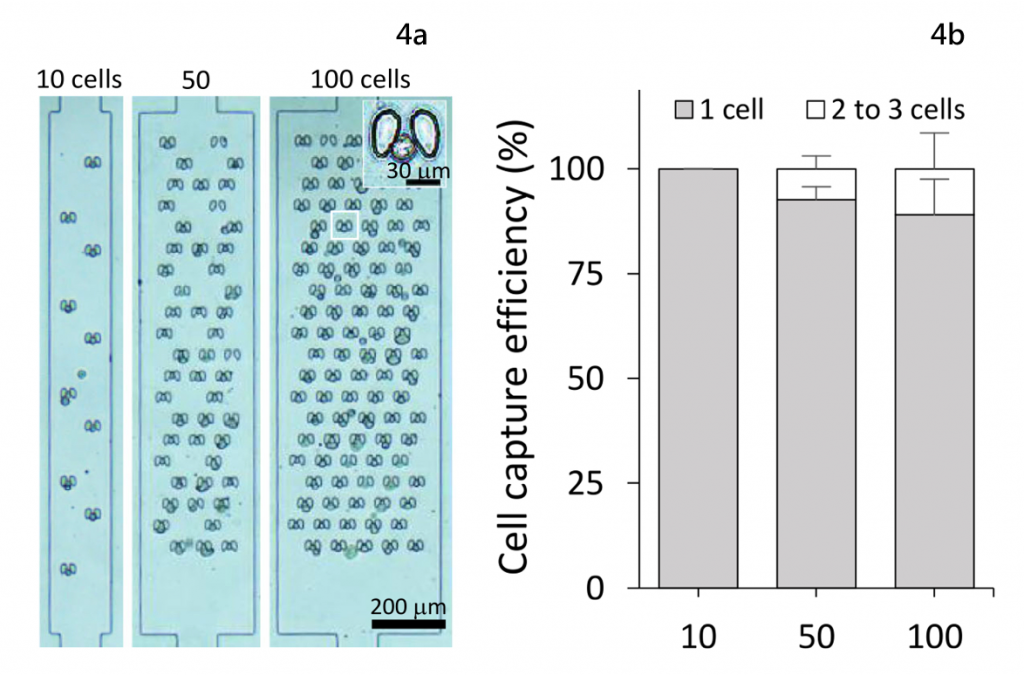
圖4. 4a.捕捉槽與被捕獲PC-9肺癌細胞影像,4b.捕捉槽數量10、50、100之細胞捕獲效率
質譜儀檢測—非數據依賴擷取方法(DIA)與客製化譜資料庫
質譜儀在檢測過程中,可以對分析離子進行二次碰撞,使胜肽片段形成更小的碎片,並再次進行掃描以獲得更多樣品資訊。使用非數據依賴擷取法 (Data-Independent Acquisition,DIA) 質譜儀分析技術,藉由掃描指定質量範圍縮小目標碎片數量,並以連續區段偵測方式同時檢測多個離子碎片,在質譜儀掃描能力的限制下,大幅增加分析目標的偵測數量,獲取最詳盡的樣品資訊,此外,陳玉如博士研究團隊除了優化儀器偵測感度,更為分析物分門別類建構客製化圖譜資料庫,以提高質譜儀對超微量蛋白質體的鑑別效率與定量可靠性。
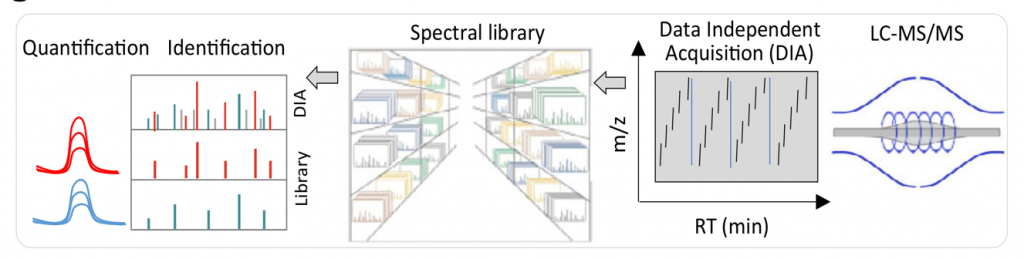
圖5. 非數據依賴擷取質譜鑑定及定量流程:1.質譜儀檢測,2.圖譜資料庫比對,3.目標胜肽定量分析
iProChip-DIA蛋白質體研究的下一步
iProChip微流體晶片與非數據依賴擷取質譜儀檢測方法,領先全球研究團隊,實現了「使用單一晶片分析單一細胞蛋白質體」的成就。iProChip針對樣品建構特製晶片,在單一晶片完成細胞捕獲、蛋白質處理、目標胜肽蒐集等前置處理,更減少過程中的損耗量,降低檢測方法對樣品數量的需求;而DIA-MS則是利用建立客製化圖譜資料庫,進行非依賴性數據圖譜比對與分析。
此一站式工作平台已經能由單一細胞鑑定出高達1500種蛋白質,並可透過後續分析,將其置於訊息網路進行相關的研究探討,且具高度可靠性與靈敏度,展示出應用於癌症細胞檢測的潛力。目前研究團隊正著手積極開發下一世代晶片,期望能將此技術用來解決重要的生物問題,亦預期此平台將有助於揭示在不同生理和病理中單一細胞調控的機理。
參考文獻
[1] T. Gebreyesusⴕ, A. A. Siyalⴕ, R. B. Kitata, E. S.-W. Chen, B. Enkhbayar, T. Angata, K.-I Lin, Y.-J. Chen* and H.-L. Tu*. Nature Communications 13, 37.(2022)
[2] Chappell, L., Russell, A. J. C. & Voet, T. Single-cell (multi)omics technologies. Annu. Rev. Genomics Hum. Genet. 19, 15–41 (2018).
[3] Kitata, R. B. et al. A data-independent acquisition-based global phosphoproteomics system enables deep profiling. Nat. Commun. 12, 2539 (2021).
[4] How can systems biology test principles and tools using immune cells as a model? Cell Syst. 6, 146–148 (2018).